Гренландские киты (bowhead whale, Balaena mysticetus)живут долго – в телах выловленных в конце двадцатого и начале двадцать первого веков, обнаруживали традиционные каменные гарпуны и фрагменты копья, относящиеся к викторианской эпохе. (https://i.imgur.com/U9QncoY.png) Если нам повезет прожить достаточно долго, лет эдак 80, даже не замахиваясь на половину китовьей биографии, то велика вероятность знакомства с раком. Каждое клеточное деление – это шанс ошибки. Больше клеток – больше делений – выше шанс ошибки. Чем ты больше и дольше живёшь. Тем, соответственно, риск столкнуться с раком.
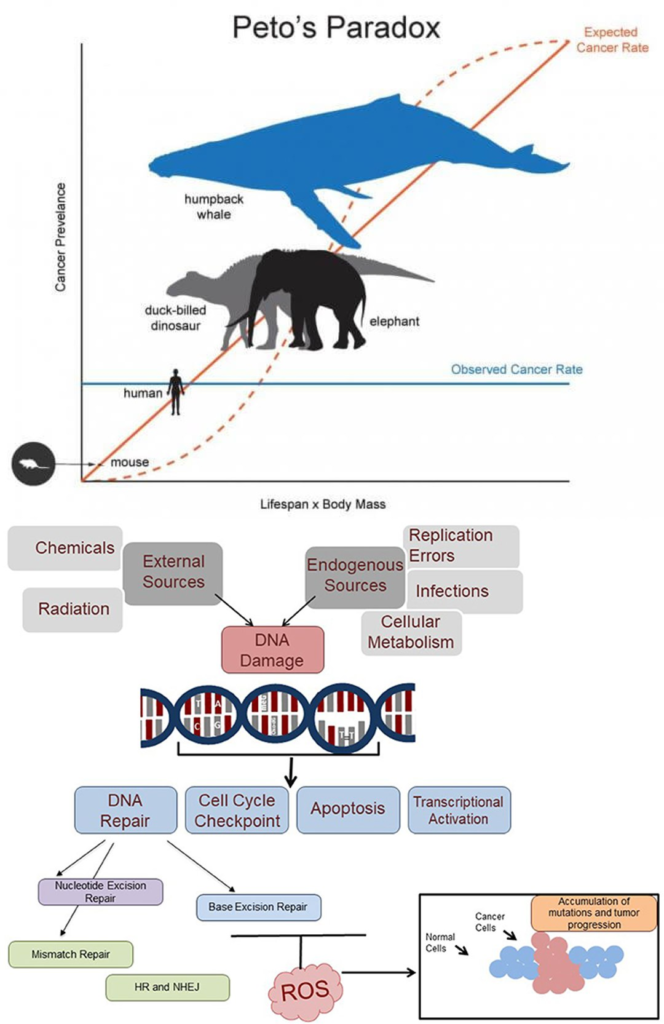
Эволюция многоклеточности потребовала подавления рака. Если каждая клетка имеет некоторый шанс стать раковой, то крупные, долгоживущие организмы должны иметь повышенный риск развития рака по сравнению с мелкими, короткоживущими организмами. Отсутствие корреляции между размером тела и риском развития рака известно как парадокс Пето. У животных, имеющих в 1 000 раз больше клеток, чем у человека, риск развития рака не увеличивается, что позволяет предположить, что естественные механизмы могут подавлять рак в 1 000 раз эффективнее, чем это происходит в клетках человека.
Когда в клетках происходят разрывы ДНК (да, такое случается неоднократно), они оказываются перед выбором: как сбалансировать краткосрочные риски для жизнеспособности организма и долгосрочные риски нестабильности генома. Одним из вариантов является “ремонт” ДНК и возобновление функционирования клетки. Если не отремонтировать разрыв двойной цепи ДНК (double strand break, DSB) то погибнет одна клетка. А вот если неточно, с ошибками отремонтировать DSB – то это может привести к возникновению рака, который убьет весь организм. Аберрантные результаты ремонта, такие как потеря фрагментов хромосом (например, микроядра), хромосомные перестройки или крупные делеции (выпадения “букв”), приводят к масштабным изменениям исходной последовательности ДНК. Эти формы нестабильности генома являются отличительными признаками рака и основными факторами злокачественной трансформации.
Масштаб этой угрозы отражается в разнообразии механизмов контрольных точек, которые эволюционировали у млекопитающих для остановки и предотвращения деления (arrest), или уничтожения клеток с повреждениями ДНК. Постоянный или чрезмерный сигнал о повреждении может вызвать вторую категорию последствий повреждения ДНК: апоптоз (запрограммированную клеточную смерть) или старение.
В популяциях клеток, находящихся в состоянии покоя (quiescent cells), существует повышенный потенциал для накопления стойких нерепарированных DSBs. Эффективное восстановление DSBs особенно важно для постоянно постмитотических клеток, таких как нейроны и кардиомиоциты, которые часто не заменяются после клеточной смерти. В конечном счете, ценность восстановления DSB для выживания организма зависит от точности и эффективности. При чрезмерном повреждении для выживания и долголетия организма лучше устранить клетки, подверженные риску геномной нестабильности, путем апоптоза или старения.
В статье описывается, каким образом киты живут долго и счастливо без рака. Вместо того чтобы обладать дополнительными генами-супрессорами опухолей как барьерами на пути онкогенеза (как можно было бы предположить), или их повышенной активностью, гренландский кит полагается на более точную и эффективную репарацию ДНК, что реализуется благодаря двум белкам, CIRBP и RPA2.
DNA repair and anti-cancer mechanisms in the longest-living mammal: the bowhead whale
